摘要
在水质测量中我们经常可以看到电导率EC,TDS,盐度等参数,但我们大部分人对他们的定义不是很了解,甚至有认为三者是同一个概念。而在土壤学领域,也有土壤盐度和土壤盐分的说法,但是至今这些方面的定义和参数源头很少有权威的说法,这导致我们在农业生产中,水质分析过程中难于统一交流,也不利于测量技术的提升。今天我们把这些基础理论和实践做一份归纳总结,希望能给大家帮助。
南京思摩特传感器有限公司,设计了新一代的SS-403土壤水温盐传感器,从实验室到悠湖,再到沿海水域进行原位校准和测量,通过这一系列实验数据分享土壤电导率测量的注意事项。
一、电导率EC
1.定义
物理学概念,指在介质中该量与电场强度之积等于传导电流密度。对于各向同性介质,电导率是标量;对于各向异性介质,电导率是张量。生态学中,电导率是以数字表示的溶液传导电流的能力。单位以西门子每米表示。电导率是表示物质传输电流能力强弱的一种测量值。当施加电压于导体的两端时,其电荷载子会呈现朝某方向流动的行为,因而产生电流。电导率 \sigma 是以欧姆定律定义为电流密度J和电场强度 E 的比率:J=\sigma E 。有些物质会有异向性的电导率,必需用 3X3 矩阵来表达(使用数学术语,第二阶张量,通常是对称的。电导率是电阻率 \rho 的倒数。在国际单位制中的单位是西门子/米:\sigma= 1/ \rho 。
2.电传导性
是物质可以传导电子的性质。按物质是否具有电传导性,可把物质分为导体,半导体和绝缘体。固态半导体的掺杂程度会造成电导率很大的变化。增加掺杂程度会造成高电导率。水溶液的电导率高低相依于其内含溶质盐的浓度,或其它会分解为电解质的化学杂质。水样本的电导率是测量水的含盐成分、含离子成分、含杂质成分等等的重要指标。水越纯净,电导率越低(电阻率越高)。水的电导率时常以电导系数来记录;电导系数是水在 25°C 温度的电导率。
3.影响因素
1)温度:电导率与温度具有很大相关性。在一段温度值域内,电导率可以被近似为与温度成正比。为了要比较物质在不同温度状况的电导率,必须设定一个共同的参考温度。
2)掺杂程度: 增加掺杂程度会造成高电导率。水溶液的电导率高低相依于其内含溶质盐的浓度,或其它会分解为电解质的化学杂质。水样本的电导率是测量水的含盐成分、含离子成分、含杂质成分等等的重要指标。水越纯净,电导率越低(电阻率越高)。水的电导率时常以电导系数来记录;电导系数是水在25°C 温度的电导率。
3)各向异性:有些物质会有异向性(anisotropic)的电导率,必需用 3X3矩阵来表达(使用数学术语,第二阶张量,通常是对称的)
4.测量原理
电导率的测量原理是将相互平行且距离是固定值L的两块极板(或圆柱电极),放到被测溶液中,在极板的两端加上一定的电势(为了避免溶液电解,通常为正弦波电压,频率1~3kHz)。然后通过电导仪测量极板间电导。
电导率的测量需要两方面信息。一个是溶液的电导G,另一个是溶液的几何参数K。电导可以通过电流、电压的测量得到。根据关系式
S=KG
可以等到电导率的数值。这一测量原理在直接显示测量仪表中得到广泛应用。而
K= L/A
A——测量电极的有效极板;L——两极板的距离;这一值则被称为电极常数。
在电极间存在均匀电场的情况下,电极常数可以通过几何尺寸算出。当两个面积为1cm的方形极板,之间相隔1cm组成电极时,此电极的常数K=1cm^{-1}。如果用此对电极测得电导值G=1000μs,则被测溶液的电导率K=1000μs/cm。
一般情况下,电极常形成部分非均匀电场。此时,电极常数必须用标准溶液进行确定。标准溶液一般都使用KCl溶液这是因为KCl的电导率的不同的温度和浓度情况下非常稳定,准确。0.1mol/l的KCl溶液在25℃时电导率为12.88ms/cm。
二、总溶解固体TDS
总溶解固体(英文:Total dissolvedsolids),又称溶解性固体总量,它表明1升水中固体(阴离子、阳离子和未分离的溶解物质)的总重量。测量单位为毫克/升(mg/L)或ppm。一般来说,优质水的含量会在 0 到 600 ppm 之间,而超过 1200 ppm 的读数通常被认为是不令人满意的 TDS 水平。我们国家标准GB5749-2006《生活饮用水卫生标准》中对饮用自来水的溶解性总固体(TDS)有限量要求:溶解性总固体≤1000mg/L。
对于真正的 TDS 测量,您需要将样品带回实验室并进行蒸发和称重操作。用 EC 直接转换为TDS不能保证准确的原因是,一些溶解的固体可能不会增加EC 读数,因此不会转换为TDS。例如,同样两杯豆浆,一杯加糖,一杯不加糖,两者的电导率基本相同,但是加糖的豆浆的TDS高出另外一杯很高。所以总溶解固体浓度TDS与水的电导率的关系不是恒定的。
从定义出发,我们可以看出总溶解固体与电导率之间的关系是水中溶解的阳离子和阴离子的类型和性质以及任何悬浮物质的性质的函数。 例如,电导率为10000 us/cm的NaCl溶液和KCl溶液,不具有相同的NaCl或KCl的样品浓度,并且它们具有不同的总溶解固体浓度。 值得注意的是,尽管严格讲使用电导率仪转换的TDS仪表仅提供估计值,但它们相当准确,您通常会发现 TDS 仪表可以满足大多数应用。
TDS(mg/L)=EC_{25℃}(\mu S/cm)\times \alpha
EC 是表征电流通过水中存在的物质的能力。TDS是表征水中的溶解固体,同时包含 EC 的颗粒以及不导电的颗粒,这是主要区别所在。因此,EC 到 TDS 的转换系数\alpha将根据样品的内容而变化,这些转换系数如果能由您的操作实验和您的仪表执行,将保障您获得适合您应用的准确值。
| 盐 | 当量电导率 | 系数\alpha |
|---|---|---|
| NaCl | 1(mg/L) TDS=2.04(uS/cm) | 0.49 |
| Na2SO4 | 1(mg/L) TDS=1.49(uS/cm) | 0.67 |
| CaSO4 | 1(mg/L) TDS=1.36uS/cm) | 0.74 |
| NaHCO3 | 1(mg/L) TDS=1.06(uS/cm) | 0.91 |
三、海水盐度
盐度的定义经历了几个阶段
1)克纽森盐度公式
在上世纪初,克纽森(Knudsen)等人建立了盐度定义,当时的盐度定义是指在 1000g海水中,当碳酸盐全部变为氧化物、溴和碘以氯代替,所有的有机物质全部氧化之后所含固体物质的总数。其测量方法是取一定量的海水,加盐酸和氯水,蒸发至干,然后在380℃和480℃的恒温下干燥48h,最后称所剩余固体物质的重量。 用上述的称量方法测量海水盐度,操作十分复杂,测一个样品要花费几天的时间,不适用于海洋调查,因此,在实践中都是测定海水的氯度,根据海水的组成恒定性规律,来间接计算盐度,氯度与盐度的关系式(克纽森盐度公式)如下:
S‰=0.030+1.8050Cl‰
克纽森的盐度公式使用时,用统一的硝酸银滴定法和海洋常用表,在实际工作中显示了极大的优越性,一直使用了70年之久。但是,在长期使用中也发现,克纽森的盐度公式只是一种近似的关系,而且代表性较差;滴定法在船上操作也不方便。于是人们寻求更精确更快速的方法。
2)重新定义
盐度与氯度的上述关系式,建立在海水组成恒比规律的基础上,这是不严格的;况且当时所取的水样,多数为波罗的海表层水,难以代表整个大洋水的规律。实际上,关系式中的常数项0.030,不符合大洋海水盐度变化的实际情况。根据海水的电导率取决于其温度和盐度的性质,通过测定其电导率和温度就可以求得海水的盐度。
1950年以后,电导盐度计的研究和发展,使盐度的测定方法得到简化,精密度也提高,比测定氯度后计算盐度的方法,更加准确和方便。因此,联合国教科文组织(UNESCO)、国际海洋考察理事会(ICES)、海洋研究科学委员会(SCOR)和国际海洋物理科学学会(IAPSO)4个国际组织联合发起,于1962年 5月召开会议,成立了海水状态方程式联合小组。此小组于1963年第二次会议上改名为“海洋用表与标准联合专家小组(JPOTS)”。经过多次讨论和研究,为了保持历史资料的统一性,将盐度公式改为
S‰=1.80655Cl‰
R.A.考克斯等对采自各大洋和海区的135个水样(深度在100米以内)的氯度值进行了准确的测定,按上述公式换算成盐度,并测定了电导比R15,得到S‰与R15关系的多项式
S‰=-0.08996+28.2970R_{15}+12.80832R^2_{15}-10.67869R^3_{15}+5.98624R^4_{15}-1.32311R^5_{15}
式中R_{15}为一个标准大气压和15°C条件下海水样品与S=35.000的标准海水电导率的比值。1966年,JPOTS推荐这多项式为海水盐度定义。同年,联合国教科文组织和英国国立海洋研究所出版的《国际海洋用表》,其中的盐度数据,就是采用上述测定电导率后换算成盐度的方法。
3)实用盐度标度
20世纪70年代以后,现场仪器如电导-温度-深度仪(CTD)等的应用,越来越多,而国际海洋用表(1966)中没有包括10°C以下的盐度数据,致使低于10°C的现场测定结果,无法统一。此外,测定了1967~1969年制备的标准海水,还发现用电导法测得的盐度,和从氯度换算得到的不一致,而出现了标准海水作为电导率标准的可靠性问题。因此JPOTS决定使用标准氯化钾溶液标定标准海水,并推荐1978年实用盐度标度。
本来,绝对盐度(SA)为海水中溶质质量和海水质量的比值,但它实际上不能直接测定,故用K15定义海水的实用盐度(S)来表达海洋观测的结果。
S=a_0+a_1K^{1/2}_{15} +a_2K_{15} +a_3K^{3/2}_{15} +a_4K^{2}_{15} +a_5K^{5/2}_{15}
其中a0=0.0080,a1=-0.1692,a2=25.3851, a3=14.0941,a4=-7.0261, a5=2.7081。
式中K_{15}是在15°C和一个标准大气压的条件下,海水样品电导率和质量比为32.4356×10^{-3}的氯化钾溶液电导率的比值。当K_{15}准确为1时,S 恰好等于35。 实用盐度值为过去盐度值的1000倍,例如,过去盐度值为 0.03512(即35.12‰),实用盐度值则为35.12。
四、土壤盐度
当前还没有完全统一的评估土壤盐度的指标,可用EC值 (µS/cm) 或TDS值 (mg/L)来表示。
1) EC和TDS的关系
一般地说,可推荐使用如下的简易计算方法:
TDS (mg/L或 ppm) = EC (dS/m)\times 640 (EC 为0.1 - 5dS/m)
TDS (mg/L 或 ppm) = EC (dS/m)\times 800 (EC > 5 dS/m)
2)饱和状态提取液EC值EC_e、实验室浸提法测定EC值EC_{1:x}、土壤溶液的EC值EC_{w}和土壤原位测量的表观电导率EC_a
现在好多学者比较支持和认同土壤盐度使用饱和状态下土壤的电导率EC_e来衡量,即土壤样品用蒸馏水进行饱和后进行测定。EC_e指标已经是植物耐盐性研究中盐度的标准测量指标,但是EC_e的获取需要更多的时间和精力来制作和获得饱和提取物,实际研究时大家经常使用较高的土壤/水比的土壤溶液提取物,即更传统的方法——通常通过各种土壤/水比(1:1、1:2和1:5)的提取液来测量土壤EC值EC_{1:1}、EC_{1:2}和EC_{1:5},然后用经验方程式转换EC_{1:1}、EC_{1:2}和EC_{1:5}为EC_e,但是许多土壤物理(例如持水量)、化学性质和物理化学过程会影响土壤水提取液的EC值EC_e,从而增加了这种转换计算的不确定性。
土壤盐度也可以通过测量土壤溶液的EC来确定EC_{w},因为通常在田间土壤含水量低于田间持水量。理想情况下,EC_{w}是土壤盐度的最佳指标,因为这部分EC_{w}是植物根部实际上吸收土壤水。Wang等认为没有被广泛使用,因为土壤EC_{w}往往还随土壤含水量而变化,并不是一个定值。
我们想象一下我们待测定的土壤的含水量接近0时的结构,它一般是多孔状的,现在我们把电极插入土壤中去,那么土壤固相多孔的结构和测量电极结构组合到一起成为“多孔电极”,现在我们加带盐的水给这个“多孔电极”,直到等效到盐水分布平衡时,并等效成我们关注的田间某一个含水量水平的盐度,那么我们从植物生理学的角度分析,应该认为EC_{w}是相关一种溶质势,当然土壤基质势\psi也决定水是否能被植物吸收,所以我们不应该将EC_{w}和\psi混淆在一起,应该进行解析。我们参考Rhoades和Bohn等的结论并进行实验验证,提出原位测量的EC_a必须同步测量土壤水分状况才可以获得EC_w和\psi,当然在盐碱地上往往含水量\psi变化不大,主要测算出EC_w就可以了。
1976年Rhoades等推导土壤电导率的宏观模型:
EC_a=\zeta\times EC_w \times \Theta+EC_s
其中EC_a是表观土壤电导率,也就是原位传感器测量获得的电导率值,EC_w是土壤溶液中电导率,\Theta是土壤含水量,\zeta是土壤传递函数包括土壤弯曲度和电极几何因子,EC_s是EC_w=0时的土壤电导率,即土壤本身颗粒表面吸附离子产生的。
1982年Bohn等推导了土壤电导率的另外的宏观模型:
EC_a=(EC_w \pi D/A\times n \times d)R_0^2+b
R_0=2\gamma/\psi
EC_a=m'/\psi^2+b'
其中D为电极间距,A为电极有效面积,d为两测量电极方向上孔隙通道中离子流过的平均间距,\gamma为表面张力,\psi土壤水张力。
2005年Wang等提出了实验室浸提法测定EC值EC_{1:x}和EC_{1:1}的关系
EC_{1:x} = x^{-n}EC_{1:1},n < 1
当x=\frac{K\%\rho_w}{(1-K\%)\rho_s}时,其对应的电导率EC为土壤饱和溶液电导率EC值EC_{sat},和饱和状态提取液EC值EC_e有等同的理论定义,可以近似相等。
3)电导率与作物之间的关系
按照美国盐土实验室1954年划分的标准,饱和含水量(高含水量)条件下的电导率EC_e与作物之间的关系如下:
<2dS/m时,对大多数作物生长无影响;
2~4dS/m时,对盐分敏感作物可能受到影响;
4~8dS/m时,大多数作物减产;
8~16dS/m时,只有耐盐作物不受影响;
>16dS/m时,一般作物都不能生长。
五、盐碱地在线测量前对电极常数的获取实践
在田间条件下,对于一定的盐土来说,在温度和土壤水分状况相同条件下,土壤电导率EC_a的变化可以反映含盐量的变化,也可以采用合适的经验公式由实测的电导率来计算土壤的可溶盐总量(TDS),但这样的计算只能是估算,它不可能与同时采土样进行实验室分析测得的TDS值相符。
仍然,在长期的定位观测中,对于盐土来说,电导率是土壤含盐量变化的重要指标。此外,对于非盐土来说,电导率所反映的离子总量可作为土壤肥力的一个综合性指标;对于受污区的土壤来说,电导率可以反映离子态污染物的消长变化,因此,电导率可以用来监测、评估土壤的污染状况。
但由于:
1)原位观测中土壤是一个连续体,我这里区别于水量平衡的连续体,这里指土壤在地球表面是一个连续的导体,也就是我们常说的土壤是地球的皮肤,所以它是一张很大很大的电阻网络;
2)采集土样到实验室的测量是从连续导体上隔断后进行测量的,所以原位测量和实验室取土测量两者的测量近视相等(这里面我们只对电信号相关的)一定有一个假设条件,即测量的空间敏感性接近。
实际电导池常数是随电导池的形状而变,对于并行的两根不锈钢棒来说,在田间土壤的实际电导测量中,待测介质是个无限大的体系,流经土体的电流线的影响范围是相当大的(尤其时盐碱地),电导池常数必须正确测定。
方法如下:先用一支已知电导池常数K1的电导电极来测量一个大水体(如池塘水)的电导L1,即可求得池塘水的电导率EC_{塘水};同样,用探针式电导传感器测量池塘水的电导L2, 显然,探针式电导池常数K2可求出,我们设计不同德容器大小进行替代以上所说德池塘,以研究尺寸效应,最终如图所示:
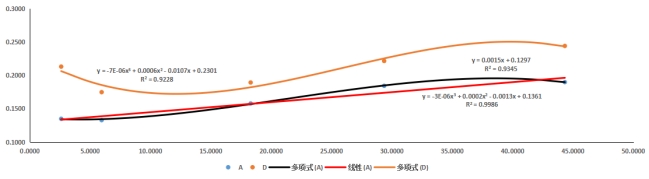
横坐标为电导,纵坐标为电极常数

a

b

c

d

e

f

g
可以得出探针式的电导率测量在大量程范围内存在电极常数随电导值的变化而变化,所以这里电极常数只能抽象为随电导变化的变量,我们指定了给出批量生产的电导传感器德电导常数-电导曲线。
比如这批次:K=aE+b,a=0.0015,b=0.1297,SS-403传感器会在生产时对每一个传感器进行电导率校准,并写入以上的参数。
SS-403传感器还支持大家对该电极常数和温度系数进行自定义,请严格参考相关说明书。
参考资料:
Soil salinity assessment using the EM38_ Field operating instruct.pdf
Salinity: Electrical conductivity and total dissolved solids.pdf
采用新电导率指标分析土壤盐分变化规律--《土壤学报》2011年04期.pdf

